MENÜ
DE | EUR
DE | EUR
-
- Alle Zentrifugen
- Tischzentrifugen
- Standzentrifugen
- Kühlzentrifugen
- Mikrozentrifugen
- Mehrzweckzentrifugen
- Hochgeschwindigkeitszentrifugen
- Ultrazentrifugen
- Concentrator
- IVD-Produkte
- Verbrauchsartikel für Hochgeschwindigkeits- und Ultrazentrifugen
- Zentrifugenröhrchen
- Zentrifugenplatten
- Gerätemanagement-Software
- Proben- und Informationsmanagement
-
- Alle Pipetten, Dispenser und automatischen Liquid-Handling-Systeme
- Mechanische Pipetten
- Elektronische Pipetten
- Mehrkanalpipetten
- Direktverdrängerpipetten und Dispenser
- Pipettenspitzen
- Flaschendispenser
- Pipettierhilfen
- Zubehör für Dispenser und Pipetten
- Automatisches Pipettieren
- Verbrauchsartikel für die Automation
- Zubehör für die Automation
- Services für Liquid-Handling-Geräte und Pipetten
Sorry, we couldn't find anything on our website containing your search term.
Sorry, we couldn't find anything on our website containing your search term.

Zellaussaatprotokoll – Leitfaden zur richtigen Aussaat von Zellen
Lab Academy
- Cell Biology
- Cell Culture
- Lab Routine
- Pipetting & Dispensing
- Reproducibility
- Pipettes
- Pipette Tips
- Essay
Die Zellaussaat ist in der Regel der erste Protokollschritt und ein Standardverfahren bei zellbasierten Versuchen. Ein korrektes und standardisiertes Protokoll für die Zellaussaat ist ein entscheidender Faktor für reproduzierbare Versuchsergebnisse. Die größte Herausforderung bei diesem Schritt besteht darin, in allen wiederholten Versuchen vergleichbare Zellzahlen zu erreichen und beizubehalten.
Dieser Artikel wurde zuerst in „Inside Cell Culture“ , veröffentlicht, dem monatlichen Newsletter für Zellkultur-Experten. Weitere interessante Artikel über CO2-Inkubatoren finden Sie auf unserer Seite „CO2-Inkubatoren – häufig gestellte Fragen und Informationsmaterial“ .
Dr. Jessica Wagener, Application Specialist Cell Handling bei Eppendorf
Die Zellaussaat ist in der Regel der erste Protokollschritt und ein Standardverfahren bei zellbasierten Versuchen. Ein korrektes und standardisiertes Protokoll für die Zellaussaat ist ein entscheidender Faktor für reproduzierbare Versuchsergebnisse. Die größte Herausforderung bei diesem Schritt besteht darin, in allen wiederholten Versuchen vergleichbare Zellzahlen zu erreichen und beizubehalten. Schwankungen in der Anzahl der ausgesäten Zellen und eine Bildung von Luftblasen während der Aussaat erhöhen die Standardabweichungen und führen zu weniger zuverlässigen Ergebnissen. Aus diesem Grund müssen bei der Erstellung eines soliden Zellaussaatprotokolls in Ihrem Labor mehrere Faktoren berücksichtigt werden.
Wenn Sie Ihre Zellen aussäen, z. B. aus einem 15-mL-Gefäß in eine Multiwell-Platte, dauert es eine gewisse Zeit, bis Sie alle Wells gefüllt haben. Unabhängig davon, ob Sie zur Zellaussaat eine Einkanal- oder eine Mehrkanalpipette verwenden, gilt: Je länger der Prozess dauert, desto mehr Zellen setzen sich im Gefäß ab. Wenn Sie die Zellsuspension im Gefäß oder Reservoir nicht mischen, wird die Zellzahl von einem Well zum anderen variieren (Abbildung 1).
Dr. Jessica Wagener, Application Specialist Cell Handling bei Eppendorf
Inhalt
- Bedeutung eines standardisierten Zellaussaatprotokolls
- Zeitfaktor und Zellsedimentation
- Video: Die richtige Pipettiermethode
- Bildung von Luftblasen
- Video: Vermeiden von Luftblasenbildung bei der Zellaussaat
- Homogene Zelladhäsion
- Bedeutung der Zelldichte
Warum ist die Zellaussaat ein kritischer Schritt bei allen Zellkulturversuchen?
Die Zellaussaat ist in der Regel der erste Protokollschritt und ein Standardverfahren bei zellbasierten Versuchen. Ein korrektes und standardisiertes Protokoll für die Zellaussaat ist ein entscheidender Faktor für reproduzierbare Versuchsergebnisse. Die größte Herausforderung bei diesem Schritt besteht darin, in allen wiederholten Versuchen vergleichbare Zellzahlen zu erreichen und beizubehalten. Schwankungen in der Anzahl der ausgesäten Zellen und eine Bildung von Luftblasen während der Aussaat erhöhen die Standardabweichungen und führen zu weniger zuverlässigen Ergebnissen. Aus diesem Grund müssen bei der Erstellung eines soliden Zellaussaatprotokolls in Ihrem Labor mehrere Faktoren berücksichtigt werden.
Der Zeitfaktor bei der Zellaussaat
Wenn Sie Ihre Zellen aussäen, z. B. aus einem 15-mL-Gefäß in eine Multiwell-Platte, dauert es eine gewisse Zeit, bis Sie alle Wells gefüllt haben. Unabhängig davon, ob Sie zur Zellaussaat eine Einkanal- oder eine Mehrkanalpipette verwenden, gilt: Je länger der Prozess dauert, desto mehr Zellen setzen sich im Gefäß ab. Wenn Sie die Zellsuspension im Gefäß oder Reservoir nicht mischen, wird die Zellzahl von einem Well zum anderen variieren (Abbildung 1). Mehr erfahren
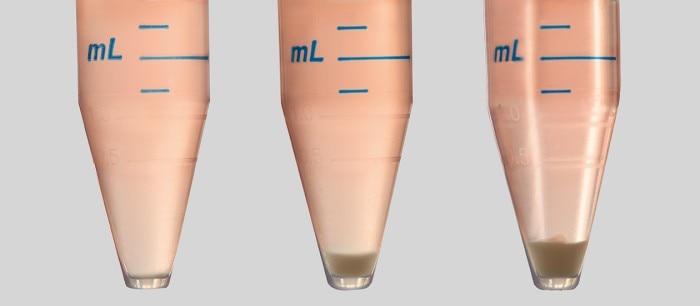
Abbildung 1: Die Zellsedimentation ist ein kritischer Faktor, der in jedem Zellaussaatprotokoll berücksichtigt werden muss. Zellen setzen sich innerhalb von nur wenigen Minuten im Gefäß ab – je länger der Aussaatprozess dauert, desto geringer wird die Zellzahl im Überstand.
Die Zellsedimentation erfolgt sehr schnell, innerhalb weniger Minuten. Um diesen Effekt zu vermeiden, müssen Sie die Zellen vor der Aussaat resuspendieren oder mischen, um sie in Bewegung zu versetzen und eine homogene Lösung zu erzeugen. Auf diese Weise wird eine gleiche Zellzahl pro Well sichergestellt.
Video: Die richtige Pipettiermethode bei der Zellaussaat
Mehr erfahren
Videos not loading, because cookies have been rejected. Change your

Bildung von Luftblasen bei der Zellaussaat
Zellkulturmedien neigen aufgrund des hohen Proteingehalts des zugesetzten Serums zur Schaumbildung. Luftblasen können die Zelladhäsion während der Aussaat behindern und daher zu Schwankungen der Zellzahlen von Well zu Well führen (Abbildung 2). Besonders in kleineren Plattenformaten wie 96- und 384-Well-Platten können Luftblasen aufgrund der kleinen Wachstumsfläche pro Well große Auswirkungen haben. Obwohl das Resuspendieren oder Mischen notwendig ist, sollten Sie es also nicht übertreiben und nicht zu viel pipettieren, um die Bildung von Luftblasen zu reduzieren. Sanftes Pipettieren reduziert auch die Scherkräfte und den Stress für Ihre Zellen – ein kritischer Bestandteil jedes Zellaussaatprotokolls.Mehr erfahren
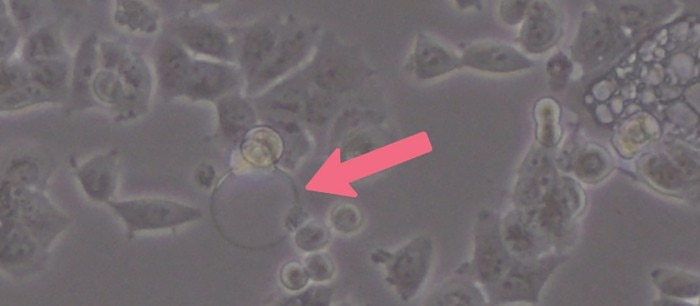
Abbildung 2: Luftblasen, die sich während der Zellaussaat bilden, können die Zelladhäsion behindern. Wie Sie sehen, können sich die Zellen in der Nähe der Luftblase nicht richtig an den Gefäßboden anlagern
Video: Vermeiden von Luftblasenbildung bei der Zellaussaat
Mehr erfahren
Videos not loading, because cookies have been rejected. Change your

Homogene Zelladhäsion
Neben einer gleichmäßigen Zellzahl kann auch eine homogene Verteilung der Zellen auf der Wachstumsfläche eines Kulturgefäßes einen Einfluss auf das Versuchsergebnis haben. Hierfür gibt es verschiedene Methoden, die in der Regel von erfahreneren Wissenschaftlern in einem Labor an ihre Auszubildenden weitergegeben werden. Aber was ist die beste Methode, um die Zellen gleichmäßig auf der Wachstumsfläche zu verteilen? In Abbildung 3 sehen Sie einen Vergleich verschiedener Methoden.Links können Sie sehen, was passiert, wenn Sie das Gefäß mit Zellkulturmedium befüllen und die Zellen dann einfach nur hineingeben: Die Zellen haften hauptsächlich in der Mitte des Gefäßes. Um eine gleichmäßige Zellverteilung zu erreichen, schwenken manche Wissenschaftler die Platten oder Schalen in Form einer Acht, während andere eine kreuzförmige Bewegung bevorzugen. Beide Methoden führen zu einer besseren Verteilung der Zellen. Je kleiner jedoch der Gefäßdurchmesser ist, desto geringer ist die Bewegung der Flüssigkeit, was zu einer ungleichmäßigen Verteilung der Zellen führt. Eine gute Methode, diesen Effekt bei der Zellaussaat zu vermeiden, besteht darin, die Zellsuspension zunächst in einem Gefäß oder Reservoir auf die gewünschte Konzentration zu verdünnen (Mastermix) und dann das Endvolumen in einem Schritt in das Kulturgefäß zu pipettieren.
Mehr erfahren
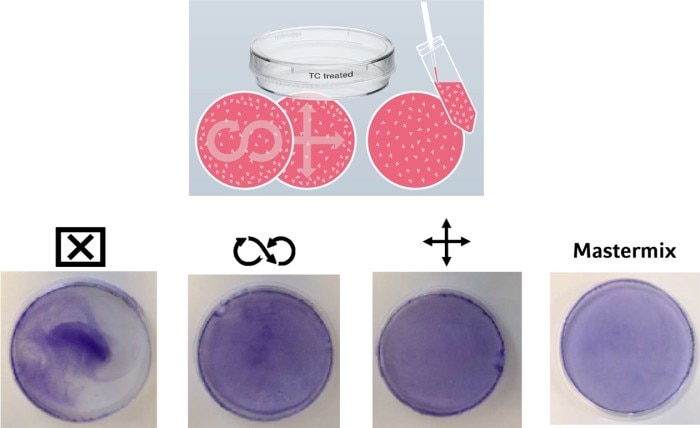
Abbildung 3: Um nach dem Transfer in das Kulturgefäß eine homogene Zelladhäsion zu erreichen, existieren verschiedene Methoden. Allerdings sind nicht alle gleichermaßen effizient. Empfohlen wird die Verwendung eines Mastermixes mit der endgültigen Zellkonzentration. Die Zellen wurden fixiert und mit Kristallviolett gefärbt.
Spielt die Zelldichte eine Rolle?
Die Homogenität der Zellverteilung kann einen erheblichen Einfluss auf Ihren Versuch haben. Natürlich gibt es Zelltypen, die dazu neigen, in Kolonien zu wachsen, statt eine homogene Monolage zu bilden. Generell sollten sich die Zellen jedoch möglichst gleichmäßig über die gesamte Wachstumsfläche des Kulturgefäßes verteilen. Ein Beispiel, das den direkten Einfluss der Zellverteilung und der zellulären Reaktionen zeigt, ist die Transfektionseffizienz (Abbildungen 4 und 5).Mehr erfahren
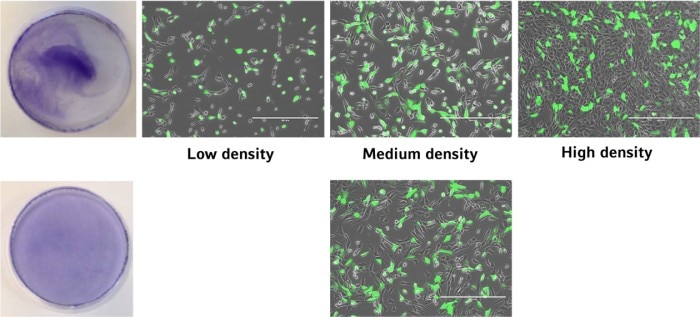
Abbildung 4: GFP-transfizierte Zellen in verschiedenen Bereichen einer Zellkulturschale nach Anwendung von zwei Zellaussaatmethoden.
Wie aus dem Diagramm hervorgeht, wird das höchste Verhältnis von transfizierten zu nicht transfizierten Zellen bei mittlerer Zelldichte erreicht. Darüber hinaus ergibt sich eine gleichmäßige Transfektionseffizienz aus einer gleichmäßig verteilten Zellschicht, die durch Anwendung der Mastermix-Methode erzeugt wird. Die Berücksichtigung beider Faktoren in einem Zellaussaatprotokoll optimiert die Transfektionseffizienz und reduziert die Standardabweichung.
Mehr erfahren
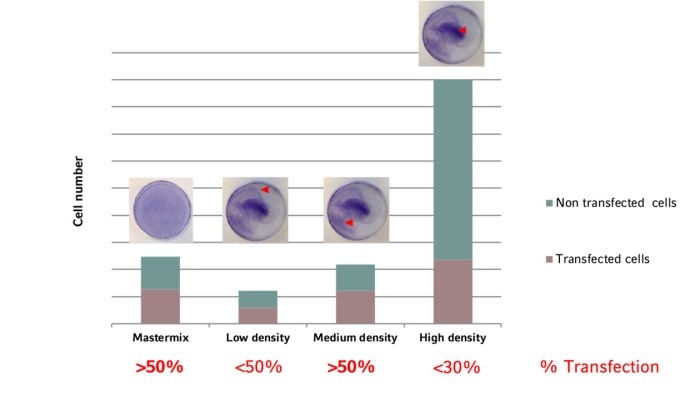
Abbildung 5: Die Transfektionseffizienz hängt von der Zelldichte ab. Die optimale Transfektionsrate und eine homogene Verteilung werden bei mittlerer Zelldichte in Kombination mit einem Mastermix-Ansatz erreicht.
